资讯详情
返回资讯目录2024年以来,不少中国创新药企业持续通过在研产品的全球申报,致力于推进创新成果造福全球病患。根据即刻药数数据,2024年第一季度有至少13项中国新药管线获得美国FDA授予快速通道资格(Fast Track Designation, FTD),以及至少14项中国新药管线获得FDA授予孤儿药资格(Orphan Drug Designation, ODD)。
值得一提的是,与2023年第一季度相比,今年第一季度获得以上两项资格认定的中国新药在研管线同比增长了3倍(2023年第一季度共计9项),呈现出加速趋势。尤其在抗体偶联药物(ADC)繁花盛开的当下,前述两项名单中有9项为ADC管线。
13项FDA快速通道资格,ADC产品为主力
在13款获得FDA授予快速通道资格的产品中,8项为抗体偶联药物(ADC),占比达到62%。从这些ADC药物的靶点和作用通路来看,包括CD79b、HER3、FRα、MSLN、Nectin-4、TROP-2和TF等。
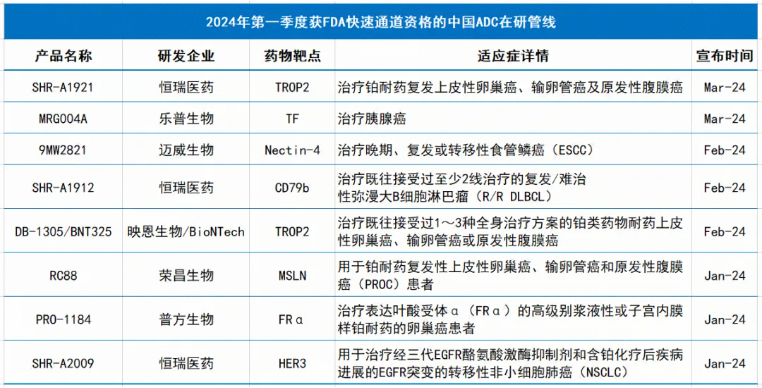
以下梳理这些ADC产品管线的临床进展以及最新披露的研究数据:
SHR-A1921:一款以TROP2为靶点的ADC。它可以与表达TROP2的肿瘤细胞特异性结合,经肿瘤细胞内吞后在溶酶体内水解释放小分子毒素,从而诱导肿瘤细胞凋亡。SHR-A1921还具明显的旁观者效应,可有效杀伤对靶细胞旁的TROP2表达阴性的肿瘤细胞。该药物用于铂耐药复发上皮性卵巢癌治疗的临床申请已获得FDA许可。
MRG004A:一款靶向组织因子(tissue factor,TF)的ADC。该产品早前已分别在中国、美国获得临床批准,并获FDA授予孤儿药资格。目前它正在美国及中国进行1/2期临床研究,并在胰腺癌、三阴性乳腺癌及结直肠癌等适应症中观察到抗肿瘤活性信号。
9MW2821:一款靶向Nectin-4的ADC。根据迈威生物新闻稿,截至2024年2月20日,9MW2821在2期临床1.25mg/kg剂量组下,单药治疗并完成至少一次肿瘤评定的30例晚期食管癌患者的客观缓解率(ORR)和疾病控制率(DCR)分别为30%和73.3%,其中28例接受过化疗及免疫治疗。该研究仍在继续入组和评估。
SHR-A1912:一款以CD79b为靶点的ADC。它可以与表达CD79b的肿瘤细胞特异性结合,经肿瘤细胞内吞后在溶酶体内水解释放小分子毒素,诱导肿瘤细胞凋亡。此次该药物获FDA快速通道资格,用于治疗既往接受过至少2线治疗的复发/难治性弥漫大B细胞淋巴瘤(R/R DLBCL)。DLBCL是非霍奇金淋巴瘤(NHL)的常见亚型。此前SHR-A1912治疗B细胞NHL的研究已在美国获批临床。
DB-1305/BNT325:一款靶向TROP2的新一代ADC。一项正在铂类药物耐药上皮性卵巢癌、输卵管癌或原发性腹膜癌患者中进行的一项1/2期研究初步数据表明,其在标准治疗失败、既往接受过多线治疗的TROP2表达实体瘤患者中表现出良好的抗肿瘤活性,ORR为30.4%,DCR为87.0%。
RC88:一种新型间皮素 (MSLN) 靶向ADC,结构包括MSLN靶向抗体、可裂解连接子以及小分子细胞毒素。它可通过靶向结合MSLN阳性的肿瘤细胞,介导抗体的内吞,从而将细胞毒素定向传递给癌细胞,实现肿瘤杀灭。RC88获FDA快速通道资格,用于治疗铂耐药复发性上皮性卵巢癌、输卵管癌和原发性腹膜癌。在此之前,该产品针对上述适应症的国际多中心2期临床研究已获得FDA许可。
PRO1184 (Rina-S):一款以叶酸受体α(FRα)为靶点的ADC。此次该药物获得FDA快速通道资格,用于治疗表达FRα的高级别浆液性或子宫内膜样铂耐药的卵巢癌。根据2023年11月公布的初期剂量爬坡数据,在可耐受剂量下,该药物在既往接受过多线治疗并未经筛选FRα表达水平的卵巢癌和子宫内膜癌患者中展现出良好的抗肿瘤活性。
SHR-A2009:一款靶向HER3的ADC。该产品已推进至2期临床,其治疗实体瘤的国际多中心1期临床研究正在开展。根据2023年10月在欧洲肿瘤内科学会(ESMO)大会上的数据,在全瘤种中的ORR为25.0%,DCR为72.2%,中位DoR为7.0个月。NSCLC患者中,ORR为30.0%,DCR为76.7%,中位DoR为7.0个月(94.4%EGFR突变;80.6%患者对3代EGFR-TKI耐药),且SHR-A2009表现出可耐受和可控的安全性。
除了以上ADC在研管线,还有其他一些类型的管线也在第一季度获得了FDA授予的快速通道资格,包括百吉生物TIL疗法、凡恩世的Claudin18.2/CD47双抗、亦诺微医药的溶瘤病毒产品、科伦药业的RET小分子抑制剂、以及华津生物的溶瘤细菌生物制品等。
14项FDA孤儿药资格,癌症管线占半壁江山
从产品类型来看,获得FDA孤儿药资格的14款在研管线包含了小分子、抗体、ADC、CAR-T疗法、基于CRISPR的AVV疗法、干细胞疗法,以及蛋白质类药物等。
从疾病治疗领域来看,有7款产品(8项认定)的适应症为癌症,占比57%。这些适应症涉及胃癌、慢性粒单核细胞白血病、恶性脑胶质瘤、间变性大细胞淋巴瘤等难治性癌症类型。
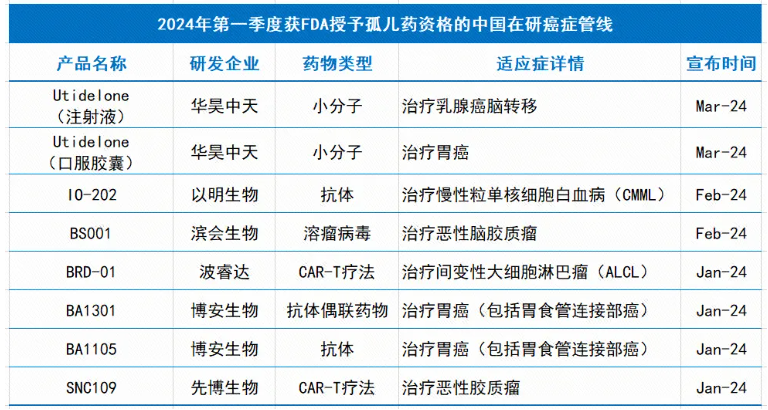
除了以上肿瘤适应症,获得FDA孤儿药资格的管线还覆盖了一些其它疾病领域。例如:迈威生物的铁稳态大分子调节药物9MW3011,用于治疗真性红细胞增多症;辉大基因的DNA编辑疗法HG302,用于治疗杜氏肌营养不良(DMD);方拓生物的AAV基因治疗产品FT-002,用于治疗RPGR基因变异引起的遗传性视网膜营养不良(IRD);领诺医药的重组酶替代疗法LIN-2003,用于治疗异染性脑白质病(MLD);睿健医药的干细胞疗法NouvSight 001,则是针对视网膜色素变性系列适应症;以及礼邦医药在研新药AP303,用于治疗常染色体显性多囊肾病(ADPKD)等等。
参考资料来源:
[1]即刻药数
[2]各家公司公开新闻稿
免责声明:
本文仅供专业人士学术交流探讨,不作为诊疗及用药依据。
如有侵权,请联系我们删除。