资讯详情
返回资讯目录

仑伐替尼(Lenvatinib)是卫材株式会社(简称卫材)自主研发的多靶点受体酪氨酸激酶抑制剂(VEGF受体-1,2,3;FGF受体-1,2,3,4;PDGFRα;RET和KIT),已于2015年获美国食品药品监督管理局(FDA)和欧洲药品管理局(EMA)批准用于侵袭性、局部晚期或转移性分化型甲状腺癌的治疗, 并于2016年FDA和EMA相继批准仑伐替尼联合依维莫司治疗晚期肾细胞癌。
今年ASCO年会上发布了仑伐替尼对比索拉非尼一线用于不可切除的肝细胞癌的III期临床试验REFLECT研究结果。REFLECT研究是一项全球多中心、开放标签、随机、非劣效III期临床试验,在954例不可切除肝细胞癌患者中对比仑伐替尼和肝细胞癌标准治疗药物索拉非尼一线治疗肝细胞癌的有效性和安全性,其中中国(含大陆、台湾省、香港特区)患者近300例,非劣效性的临界值为1.08。
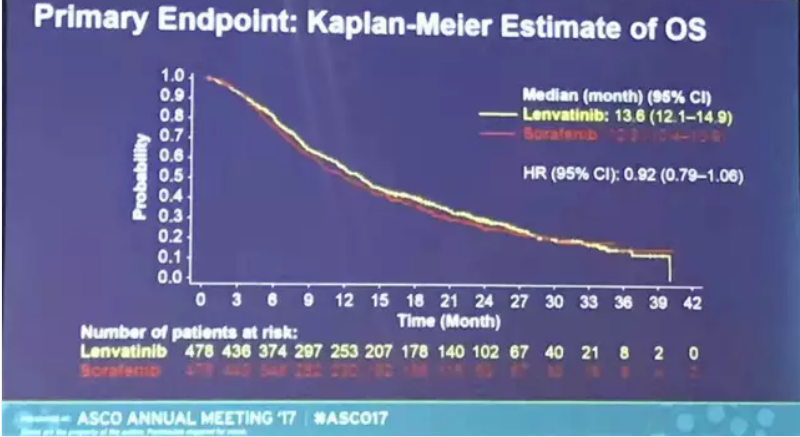
结果显示,仑伐替尼同索拉非尼相比,在主要研究终点,即中位总生存(OS)方面达到非劣效性的统计标准(13.6个月 vs. 12.3个月,风险比(HR)为0.92,95%置信区间 [CI] = 0.79-1.06)。
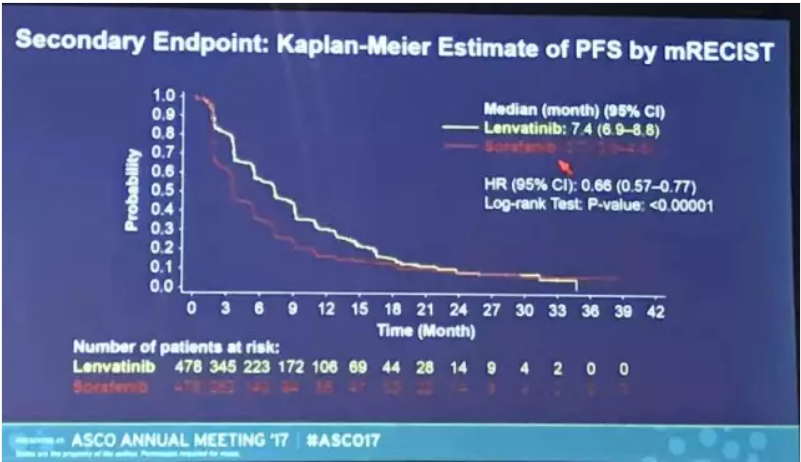
此外,仑伐替尼在中位无进展生存期(PFS)(7.4个月 vs. 3.7个月,P<0.00001),中位疾病进展时间(8.9个月 vs. 3.7个月,P<0.00001)和客观缓解率(24.1% vs. 9.2%,P<0.00001)三个次要研究终点方面显著优于索拉菲尼。
在安全性方面,仑伐替尼组最常见的5种不良反应为高血压、腹泻、食欲减退、体重减轻和乏力,均与之前的报道结果一致。基于REFLECT的研究结果,卫材已与今年6、7月份相继向日本、美国和欧州提交了仑伐替尼用于治疗肝细胞癌的监管申请。
目前原发性肝癌是我国第4位常见恶肿瘤,占肿瘤致死原因的第3位[1],其中肝细胞癌(HCC)最常见,占85%~90%以上。2012年全球肝癌新发病例和死亡病例一半以上发生在中国[2],其中乙型肝炎病毒(HBV)慢性持续感染是我国HCC最重要的危险因素,BRIDGE研究显示有77%的中国HCC患者存在HBV感染[3]。
早期HCC患者可采用手术、射频消融、无水酒精注射、栓塞化疗等各种治愈性方案,但早期HCC症状隐匿,多数患者确诊时已属中晚期,丧失了根治性治疗的机会。晚期HCC患者治疗方法有限且预后差,唯一可选择的靶向药物索拉菲尼对患者总生存期(OS)的改善易受肝炎病毒感染的影响,其并不能改善HBV阳性及HCV阴性患者的OS[4]。
此外,中国人口基数大, HCC的新发病例仍持续上升,且晚期和合并HBV的患者比例高,因此临床仍急需疗效好且对HBV相关肝癌有效的新型药物。
可喜的是,针对REFLECT研究的中国患者亚组分析结果显示,仑伐替尼对中国肝癌患者、HBV相关肝癌患者的总生存期显著优于索拉非尼,仑伐替尼有望成为中国晚期肝细胞癌患者一线治疗的新选择。
解放军八一医院全军肿瘤中心的秦叔逵教授将在第二十届全国临床肿瘤学大会暨2017年CSCO学术年会上报告了REFLECT试验最新的中国患者亚组分析结果,敬请期待!
免责声明:
本文源自转载文章,仅供专业人士学术交流探讨,不作为诊疗及用药依据。
如有侵权,请联系我们删除。